

Das vegetative Nervensystem (VNS) ist phylogenetisch älter als das zentrale Nervensystem (ZNS) mit Gehirn und Rückenmark. Es wird auch als autonomes Nervensystem bezeichnet, da es ohne willkürlichen Einfluss durch das menschliche Denken, also den bewußten Willen funktioniert.
Man findet in der Literatur u.a. Medien Beweise über das Vorhandensein von Nervenzellen bei niederen Tieren wie Hohl- bzw. Nesseltieren, wo es als Netz in der Haut liegt. Aber auch hier besteht schon eine Spezifizierung in Nervenzellen für die Bewegungsfunktion (Einfangen von Nahrung) und für die Speicherung von Informationen (Konzentration besonders empfindlicher Zellen am Kopfende). Bei Würmern ist dann ein Strickleitersystem und die weitere Trennung zwischen Kopf- und Bauchhirn erkennbar. Die Weichtiere besitzen ein lernfähiges Hirn und ein vegetatives Nervensystem mit einem „miterregendem“ Sympathikus, welcher bei Gefahr sofort reagiert (Fluchtverhalten). Bei den Gliedertieren, wozu auch die Fruchtfliege (drosophila) gehört, erfolgt eine stärkere Segmentierung sowie Knotenbildung (Ganglien). Ein auf die Verdauung spezifiziertes enterisches Nervensystem (ENS) arbeitet schon unabhängig, und neurosekretorische Zellen bilden ein primitives Hormonsystem. Schließlich erfolgt bei den Wirbeltieren eine beschleunigte Entwicklung und weitere Funktionsteilung des VNS in ein enterisches, (ortho)sympathisches und parasympathisches System. Bei den Säugetieren ist im Vergleich zu Reptilien eine Weiterentwicklung der Orientierungsreflexe sowie Kommunikation gefunden worden. Man führt dies auf die Existenz und Verschaltung nicht nur des limbischen Systems, sondern der Hirnstamm-Kerngebiete wie Ncl. ambiguus und tractus solitarius zurück. [11] Nach der von Ernst Haeckel (1834-1919, besuchte ab den 40er Jahren u.a. das Domgymnasium in Merseburg) erstmals formulierten biogenetischen Grundregel rekapituliert sich diese Phylogenese in der Ontogenese des Menschen.
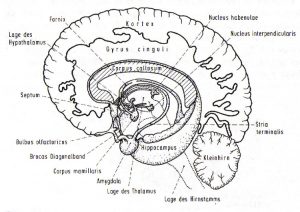
Abb.1 aus [2]
Die Funktion der Nervenzellen bzw. Neurone wird durch die Synapsen bzw. postsynaptischen Rezeptoren bestimmt. Mittlerweile sind zahlreiche Subtypen dieser Rezeptoren bzw. Neuro- u.a. Transmitter nachgewiesen worden. So findet man Neurone, welche Signale in verschiedene Richtungen orthograd und retrograd weiterleiten und solche, die diese hemmen. Dies liegt am Bau der Tubuli, intrazellulären Botenstoffen und an der Art der Verschaltung zum benachbarten Neuron (End-zu-End, End-zu-Seit bzw. End-zu-Soma). Andererseits können sie durch exhibitorisch und inhibitorisch wirkende Transmitter Impulse verstärken oder hemmen [1]. Verschiedene Netzwerke prägen schließlich die Funktion verschiedener Teile des Nervensystems. Die Funktion des VNS ist dabei stark von Impulsen des Subcortex bzw. limbischen Systems (Hippocampus, Gyrus cinguli und Mandelkörper bzw. Amygdala), wo alle Lernvorgänge im Laufe des gesamten Lebens gespeichert werden, geprägt (Abb. 1 aus [2])
Dreh- und Angelpunkt ist der Hypothalamus im Zwischenhirn. Die Steuerung erfolgt in den verschiedenen Kerngebieten, wobei man rostrale Kerne von medialen, lateralen und kaudalen Kernen unterscheidet. Sie regulieren spezifisch sympathische bzw. ergotrope oder parasympathische bzw. trophotrope oder Reaktionen.
Eine Verschaltung mit den vegetativen Kernen des Sympathikus in den Seitenhörnern des Rückenmarks und denen des Parasympathikus im Mittelhirn erfolgt vom Corpus mamillare über den Tractus mamillotegmentalis bzw. Fasciculus longitudinalis posterior Schütz zu retikulären Mittelhirnstrukturen (Formatio reticularis). Hier befinden sich wichtige Kerngebiete (Ncll. raphe, tegmentalis, ambiguus, tractus solitarius und der Locus coeruleus), welche für Raumorientierung, Koordination der Nahrungsaufnahme, Verdauung und Ausscheidung, Atmung, Herz-Kreislauf, aber auch Kommunikation, Mimik und Gestik zuständig sind. Im aufsteigenden bzw. aszendierendem retikulärem aktivierendem System (ARAS) der Formatio reticularis werden zusätzlich Bewusstseinslage bzw. Wachheitszustand und somit die Sensibilität gegenüber Schmerz, allen Afferenzen, optischen und akustischen Reizen gesteuert. [3,4] Eine weitere Verschaltung findet über Interneurone bis zum Sacralmark statt.
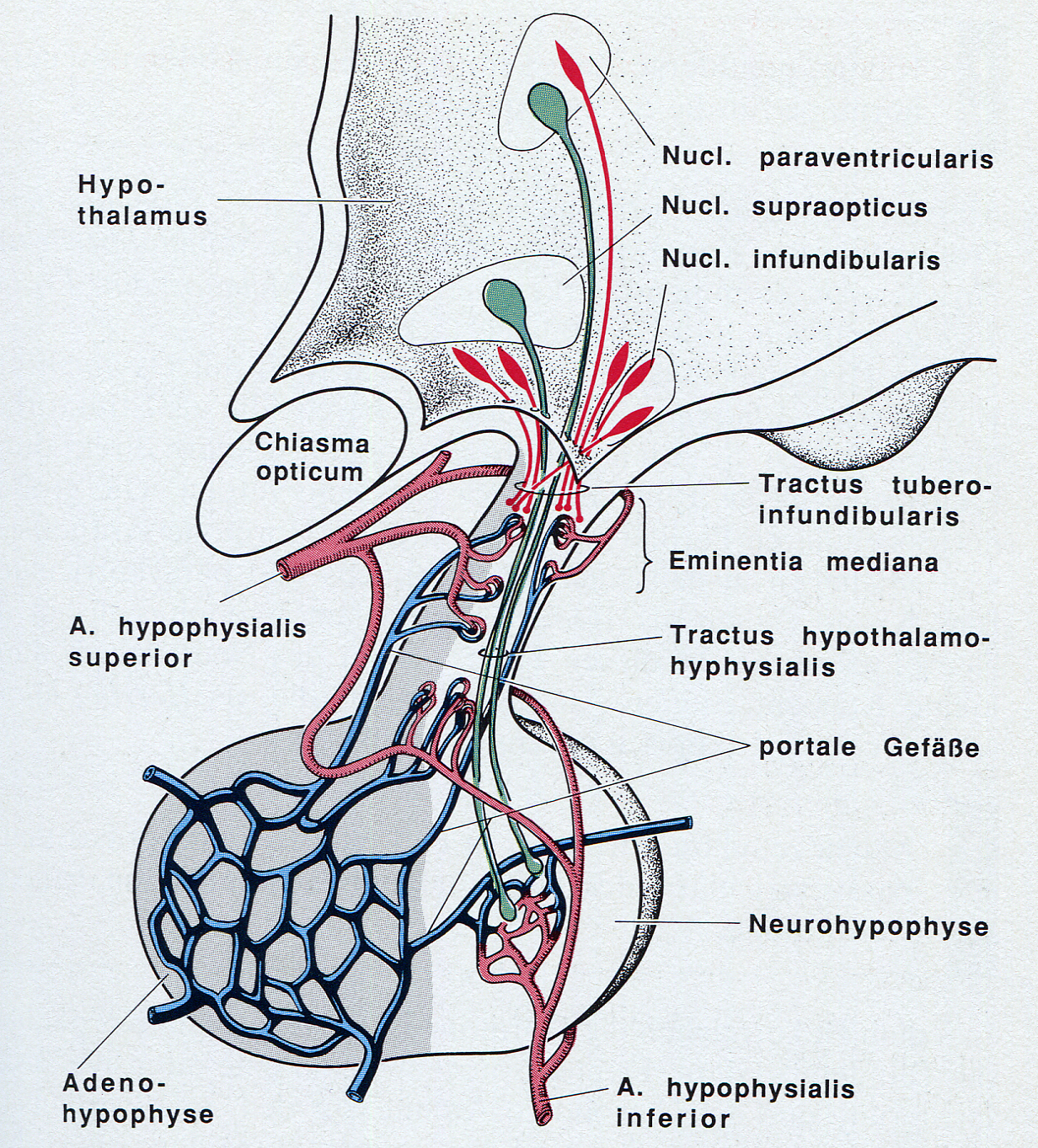
Abb.3 aus [5]
Histochemisch dominieren zentral als Transmitter Acetylcholin (cholinerges System) und beim monoaminergen System Noradrenalin (adrenerg) bzw. Dopamin (dopaminerg) sowie Serotonin (serotonerg). Darüberhinaus fand man GABA-erge, glutaminerge, histaminerge und weitere peptiderge (z.B. Neuropeptid Y) Synapsen. Noradrenerge (u.a. im Locus coeruleus) und serotonerge Kerne (u.a. Raphé-Kern) beeinflussen sich zentral dabei sehr stark. Dopamin wurde auch im Tegmentum (Abb. 4 aus [6]), in sympathischen Ganglien und der Nebenniere nachgewiesen. [7] Peripher dominieren das cholinerge und adrenerge System mit nicotinergen und muscarinergen sowie alpha- und beta-adrenergen Subtypen.
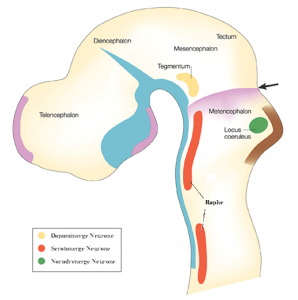
Abb.4 aus [6]
Der „Mit-Erreger“ wird auch als Hauptsympathikus bzw. nur als Sympathikus bezeichnet. Sein erstes Neuron ist kurz und sein zweites lang. Dieses befindet sich außerhalb des ZNS.
Die zentrale Bahn beginnt wahrscheinlich auch im Hypothalamus. Cholinerge und dopaminerge Verbindungen wurden bis zu den Zellkernen des 1. bzw. präganglionären Neurons in den Ncl. intermediolaterales der Seitenhörner des Rückenmarks (RM) nachgewiesen. [7] Die Topographie der Kerne wird von C7 oder C8 bis L2 oder L3 angegeben (siehe Literatur der topographischen Anatomie).
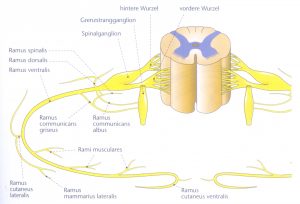
Abb. 5 aus [8]
In diesen Ganglien erfolgt entweder die Umschaltung von prä- auf postganglionäre Fasern über Acetylcholin oder der „Durchlauf“ zu anderen unpaaren prävertebralen, präaortalen bzw. peripheren Ganglien. [4,8]
Nach cholinerger Umschaltung verlaufen zahlreiche Fasern erst entlang des Grenzstrang nach kranial oder kaudal (bis zu 5 Segmenten) und dann über Verzweigungen in andere Segmente oberhalb C8 und unterhalb L2 (primäre Divergenz des Grenzstrangs). Da diese Verzweigungen nicht myelinisiert sind, erscheinen sie als Rr. communicantes grisei (also grau). Nun verzweigen sich die Nn. spinales nochmal in die Peripherie über rami dorsales und ventrolaterales (sekundäre Divergenz der Spinalnerven). Dadurch gelangen sympathische Impulse entlang der Nerven und schließlich Gefäße (tertiäre Divergenz der Gefäße) in die Peripherie. So ist die sympathische Versorgung durch die Kerngebiete über andere Segmente in die Regionen von Kopf-Hals (C8-D3), Armen (D3-7), Becken (D10-12) und Beinen (L1-3) gewährleistet. [4,8]
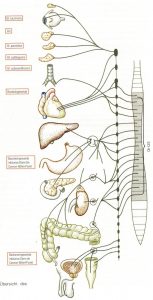
Abb. 6 aus [3]
Vernetzungen des Grenzstrangs bestehen cervical zum prävertebralem Plexus caroticus et thyroideus. Über das GCS gibt es Verbindungen zu Art. carotis, Nn. trigeminus, glosspharyngeus, vagus et hypoglossus sowie phrenicus und weiter zu Ggl. ciliare, N. petrosus major und Ggl. spheno(pterygo)platinum (Palatinum). Über das Stellatum erreichen Fasern N et Art. vertebralis, Nn. vagus, laryngeus recurrens und Art. subclavia. [4]
Im thorakalen Teil bestehen Verbindung zu prävertebralen Plexus cardiacus, pharyngeus, pulmonalis, coeliacus und zu einem gel. vorkommednen Pl. splanchnicum. [4]
Lumbal sind die Plexus aorticus abdominalis, mesenterialis und hypogastricus superior sowie sacral der Plexus hypogastricus inferior vernetzt. [4]
Weiterhin ziehen sympatische Fasern als Nn. splanchnici major (beginnt an den Grenzstrangganglien Th5-9) et minor (Th10-11), gel. auch imus (Th12) in das prävertebrale Ggl coeliacus (besser Plexus) und dann zur Niere als Plexus renalis. Als Nn. splanchnici lumbales et sacrales verlaufen Fasern in die Peripherie und anastomosieren variabel mit dem Parasympathikus (z.B. im Plexus hypogastricus). [4]
Ohne nachgewiesene Bedeutung sind Paraganglien wie das sich zurückbildende Zuckerkandl-Organ an der Art. mes. inf. sowie andere chromaffine Paraganglien in Drüsen und dem Peritoneum.
Eine Sonderrolle spielt das umgewandelte sympathische Ganglion „Nebennierenmark“. Ohne Umschaltung im Grenzstrang wird über die Segmente Th10-L2(3) bei jeglichem Stress (Schmerz, Verletzung, Hypotension und Hypothermie sowie starke Angst) über die sympathiko-medulläre Achse (SMA) in Sekundenschnelle Adrenalin aus dem Nebennierenmark für die adrenerg versorgten Organe bereitgestellt, um der Gefahr phylogenetisch gerecht zu werden (fight or flight). [8,9]
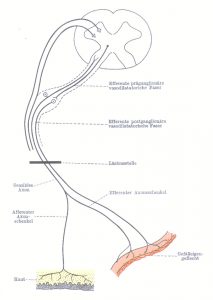
Abb. 7 aus [8]
Durch Nozizeptoren von freien Nervenendigungen im Bindegewebe (extrazelluläre Matrix), Thermorezeptoren oder Mechanorezeptoren glatter Muskelzellen (besonders der Gefäße und Hohlorganen) gelangen Signale aus der Peripherie nach zentral sowie Noradrenalin endokrin an α1-Rezeptoren [9]. 80% aller sympathischer Afferenzen werden über den Ramus dorsales des N. spinalis in den Laminae des Hinterhorns verschaltet. Die übrigen gelangen wie der Großteil der sensorischen Afferenzen über den ventrolateralen Ast in das Hinterhorn des RM und werden nach zentral oder kontralateral weitergeleitet, gehemmt oder reflektorisch beantwortet. Die verhältnismäßig langsame Leitung erfolgt über marklose C-Fasern entlang der Gefäße, peripheren und o.g. Eingeweide-Nerven zum Grenzstrang bzw. nach „Durchlauf“ über die Spinalganglien (pseudounipolare Zellen) in die hinteren Wurzeln der Segmente C(7)8 bis L2(3). Durch diese Konvergenz werden sympathische Afferenzen zentral „unsegmental“ empfunden, jedoch über reflektorische Efferenzen polysegmental oder auch streng segmental in Dermatome als referred pain nach Head, als Verquellungen in „Subkutome“ nach Kibler, Kohlrausch, Aschner, Gleditsch etc., faszio-muskulär in Triggerpunkte nach Travell, kinetischen Muskel-Ketten nach Mackenzie bzw. als arthrogene Blockierungen projiziert.
Vorm Erreichen des N. spinalis kann aber auch ein axonaler Reflex (Abb.7 aus [8]) mit Umschaltung in Ephapsen auf eine Efferenz zu reflektorisch-vegetativen bzw. algetische Krankheitszeichen (u.a. triple response nach Lewis mit red spot (zentrale Rötung), spreading flare (Umgebungsreaktion der Gefäße) und wheal (Ödem) lokal [12] und einer so genannten neurogenen Entzündung systemisch führen, wobei hier die Substanz P eine entscheidende Rolle spielt. [8]
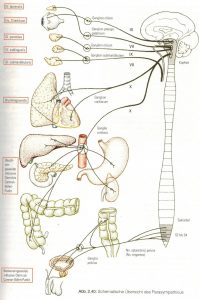
Abb. 8 aus [3]
Topographisch unterscheidet man hier die Pars encephalica von der sacralis (Abb. 8 aus [3]). Die zentralen Ursprungskerne der 1. bzw. präganglionären Neurone vom N. occulomotorius (Edinger–Westphal), chorda tympani n. facialis (salivatorius superior), glossopharyngeus (salivatorius inferior) und vagus (dorsalis n. vagi, ambiguus et tractus solitarius) befinden sich im Mittel- bzw. Rautenhirn (Abb. 9 aus [10]. [11]
Sie verlaufen weiter vagabundierend mit diesen Hirnnerven III, VII, IX und X, anderen Hirnnerven (z.B. N. trigeminus) und entlang von Gefäßen bis zu den Erfolgsorganen (z.B. Drüsen und Muskeln). Die Umschaltung von prä- auf postganglionäre Fasern erfolgt über Acetylcholin in Ganglien (Ggll. ciliare, oticum, spheno(pterygo)palatinum), submandibulare) und nicht-chromaffinen Paraganglien (Glomus caroticum et aorticum). Über den N. vagus, welcher einerseits aus dem Ncl. dorsalis n. vagi entspringt, zu Kehlkopf, Luftröhre, Bronchien, Herz und Magen sowie zum Gatrointestinaltrakt bis zum Cannon-Böhm’schen Punkt verläuft, erreicht der parasympathische Einfluss die Organe, welche für die Aufnahme von Sauerstoff und Nahrung sowie deren Verteilung verantwortlich sind. Im Rahmen der Poly-Vagal-Theorie nach Proges werden über den „smarteren“ N. vagus, welcher sich erst im Laufe der letzten Schwangerschafts- und ersten Lebensmonate entwickelt, myelinisiert ist und vorwiegend aus dem Ncl. ambiguus Impulse erhält, v.a. kommunikative und soziale Fähigkeiten wie Modulation der Muskeln von Biss (N. V), Auge und Gesicht (N. III, IV, VI und VII), Ohr (N. VIII), Rachen und Kehlkopf (N. IX) vermittelt. Dieser phylogenetisch jüngste Teil des VNS moduliert v.a. linksseitg die subdiaphragmalen Organe und rechtsseitig die o.g. supradiaphragmalen „Organe“ einschl. Sinusknoten und damit die Herzvariabilität. Ein weiterer vagaler Einfluss v.a. auf die Respiration beim Sprechen wird durch den Ncl. tractus solitarii ausgeübt. [11] Ein Einfluss besteht auch auf die vom N. accessorius (XI) versorgten Muskeln Sternocleidomastoideus und Trapezius (die häufigsten Triggerpunkte) und scheint sich durch die enge anatomische und phylogenetische Beziehung der so genannten Vagusgruppe zu ergeben.
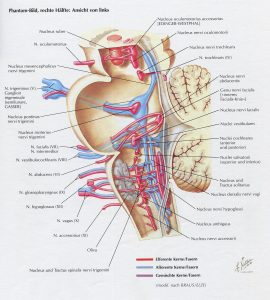
Abb. 9 aus [10]
Die cholinerge Umschaltung erfolgt meist intramural. Eine besondere Bedeutung besteht in der Verbindung zum enterischen Nervensystem (ENS), indem die Impulse des Vagus in den Plexus myentericus (Auerbach) und/oder submucosus (Meissner) umgeschaltet werden. Obwohl das enterische System prinzipiell unabhängig arbeitet, ist der Einfluss des Parasympathikus hier sehr hoch in Ruhe- oder Erhohlungsphasen (rest and digest). Im unteren Abdomen bzw. Beckenbreich, retroperitoneal sowie sacral erfolgt nicht nur die o.g. Umschaltung, sondern eine gegenseitige Beeinflussung mit dem Sympathikus in diversen ineinander gehenden Plexus (z.B. hypogastricus, prostaticus oder uterovaginalis). Somit sind Fortpflanzung und Ausscheidung stark vom Sympathikus bzw. Stress abhängig. Hier herrscht ein in der Endokrinologie bekannter Feedback-Mechanismus auf die releasing Hormone der Hypophyse vor.
Sie gelangen aus den Organen (z.B. Messung der Dehnung von Hohlräumen und Gefäßen, der Temperatur und des ph-Wertes) innerhalb von Reflexbögen (Atem-, Husten-, Brechreflex sowie Blasen-, Darm- und Genitalfunktion), wo sie segmental-reflektorisch verarbeitet werden, schließlich das ZNS. Über den myelinisierten „smarteren“ Vagus gelangen Afferenzen nicht nur aus Herz und Lunge, sondern v.a. aus den Afferenzen der Hirnnerven III-VI sowie IX und XI (Muskeln, Drüsen und Schleimhäute) in den Hirnstamm und werden über den Ncl. ambiguus, Ncl. tractus solitarius u.a. Kerne verarbeitet. Im myelinfreien N. vagus aus dem dorsalen Kern verlaufen bis zu 80% Afferenzen aus Bauch- und Brustraum [11], welche wie die zusätzlichen sacralen Impulse innerhalb des Mesenzephalon auf andere Neurone (v.a. N. V), retikuläre Strukturen und limbisches System umgeschaltet werden (Vgl. Linien nach Lähr und Sölder, Müdigkeit, Erschöpfung (Chronic Fatigue Syndrom bzw. CFS) oder Schlafstörung je nach „vollem Bauch“, „Laune“ usw.).