

Rezeptoren sind allosterische Zell(wand)proteinkomplexe zur Aufnahme, Transformation und Weiterleitung von Informationen aus der extrazellulären Matrix bzw. von einer Zelle in eine andere Zelle. Sie verfügen über spezifische molekulare Eigenschaften und Fähigkeiten zur physikochemischen Änderung und damit Auslösung einer elektrischen Aktion über Ionen (Rezeptoren und Synapsen) oder chemischen Reaktionen über second messenger (Rezeptoren und Nozizeptoren)
Elektrische Signale können durch Membran dringen oder über Liganden bzw. Ionen die Konfiguration der Rezeptoren, welche als Kanäle bzw. Poren aufgebaut sind, ändern bzw. chemische Reaktion auslösen (ionotrope Rezeptoren bzw. ligandengesteuerte Ionenkanäle). Boten- bzw. Signalstoffe sind meist zu groß für Poren, so dass Rezeptoren auf der Zelloberfläche als Bestandteil der Zellmembran fungieren (metabotrope u.a. G-Protein-gekoppelte Rezeptoren). Weiterhin sind auch Zell-Kern-Rezeptoren bekannt. [1,2,3] Eine Übersicht findet man auch bei wikibooks.org.
Es handelt sich hierbei um transmembranös angeordnete Proteinketten aus 7 Helices, welche zahlreiche Untereinheiten und pharmakologische Effekte vorweisen, dar. Man unterscheidet große heterotrimere, kleine monomere und mittelgroße G-Proteine, wobei die großen über o.g. transmembranöse Helices oder Guaninnucleotid-Austausch-Faktoren (GEF) aktiviert werden. Eine freie Untereinheit ist immer innen an die Membran gebunden und aktiv. Je nach dem Effekt unterteilt man weiter in stimulierende G-Proteine (s), inhibierende (i) und in die unspezifischen Effekten (q). Gαq steht für einen extrazellulären Reiz durch Acetylcholin oder α-Adrenergica und wirkt hemmend auf Adenylat-Cyclase (Ca-Einstrom) bzw. Phosphodiesterase sowie aktivierend auf K-Kanäle (K-Einstrom). [2,3,4,5,6,7]
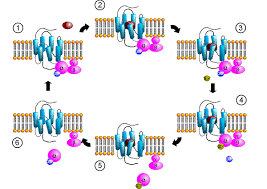
Bild eines G-Protein-Zyklus aus wikipedia.org
Neben dem eigentlichen membranösen Rezeptor sind sekundäre Botenstoffe bzw. second messenger als Kopplungselemente nötig, um die Information nach der Änderung der Konfiguration des Rezeptorproteins umzusetzen. Die intrazelluläre Signalkette verwirklicht somit die eigentliche Hormonwirkung. [1,2,3]
Das zyklische Adenosin-Mono-Phosphat (cAMP) wird meist über ein G-Protein aktiviert und steuert dann einen Kinase-Effekt (z.B. ie Phosphorylierung durch Proteinkinase A). Das trifft für Rezeptoren von GnRH, Gonadotropin, SST, ACTH, MSH, Vasopressin (nur V2-Rezeptor), Katecholaminen (nur α2, β-und Dopamin1,2-Rezeptor), PTH, Kalzitonin, Insulin, Glucagon, Gastrin, Sekretin, Histamin (H2–4-Rezeptor), Serotonin (HT1, 4-7) u.a. Kinine zu. [1,2,3]
Die Inositolphospholipid-Metabolite werden auch meist über ein G-Protein aktiviert und durch die Phospholipase C (z.B. PIP2 in Diacerylglycerol (DAG) und Inositolphosphat (IP3)) gespalten. IP3 aktiviert über Ca-Ionen aus dem endoplasmatischen Retikulum Calmodulin als tertiären Botenstoff zur Enzymaktivierung und DAG stimuliert die Proteinkinase C. Beispiele sind Rezeptoren für TRH, TSH, Oxytocin, Vasopressin (V1,3), Katecholamine (nur α1), Gastrin, Histamin (nur H1), Serotonin (nur HT3), Kinine und Angiotensin II. [1,2,3]
Zyklisches Guanosin-Mono-Phosphat (cGMP) vermittelt Reize durch andere selterne Boten wie Atriopeptin (ANP) und NO, wobei letzters direkt nach Permeation der Membran auch die Proteinkinase G aktiviert. [1,2,3]
Eine besondere Form sind die Tyrosin-Kinase-Rezeptoren. Hier ist kein second messenger nötig, da es zur Autophosphorylierung kommt. [3]
Sie nehmen chemische und mechanische Signale aus der unmittelbaren Umwelt auf und liegen v.a. in der Haut (Hautrezeptoren).
Sie registrieren die Stellung des Körpers im Raum und liegen in tieferen Schichten v.a. als Muskelspindel, Sehnenspindel bzw. Golgi-Organ.
Sie nehmen chemische und mechanische Signale aus dem Körperinneren auf und reagieren auf Dehnungsreize. Eine besondere Rolle spielen hier die Barorezeptoren der großen Gefäße.
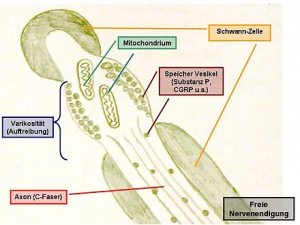
aus wikipedia.org
Dieser spezielle Rezeptor reagiert auf unterschiedliche Schmerz-Reize. Meist liegt er als freie Nervenendigung vor [1] und ist über marklose (Gruppe IV)- oder dünn markhaltige (Gruppe III)- Fasern mit dem ZNS verbunden. [8] Alle Nozizeptoren haben eine unterschiedliche Reizschwelle und kommen in Haut, Muskeln, Sehnen und Kapseln sowie in Lymph- und Gefäßwänden, im Endoneurium und in der extrazellulären Matrix des Bindegewebes vor. Sie sind nicht im Gehirn lokalisiert und schon unterm Einfluß von nerv growth factor (NGF) bereits vor der Geburt gebildet. [9]
Beim akuten Ereignis werden sie direkt durch mechanische, thermische bzw. chemische Einflüsse oder indirekt über Kinine, Histamin, H+– und K+-Ionen sowie zyklische Endoperoxide u.a. gereizt. Daraufhin setzen sie Mediatoren (Substanz P, Calcitonin gene-related-Peptide bzw. CGRP) selbst frei (neurogene Entzündung), wodurch eine (Peri)Vaskulitis entsteht. [10] Nach Traumen treten vermehrt perivaskuläre Sympathikusfasern auf, welche sensible Afferenzen (Nozizeption) nach Triggerung durch NGF modulieren. [11]
Je nach Chronizität der Reizung kommt es zur Umwandlung in echte Rezeptoren mit weiterer Erniedrigung der jeweilige Reizschwelle [9], was man als primäre Hyperalgesie [12] bezeichnet. Je nach Verlauf erfolgt die Sensibilisierung über Mg+-Ionen-abhängige NMDA(N-Methyl-D-Aspartat)-Rezeptoren durch vermehrten Einstrom von Ca++-Ionen und Aktivierung von second-messenger-Systemen (v.a. über Freisetzung von DAG und IP3) sowie Potenzierung („wind up“) weiterer Rezeptoren (z.B. AMPA(Aminohydroxy-Methylisoxazole-Propion-Säure)-Rezeptor) mit zusätzlich vermehrtem Einstrom von Na+-Ionen, was man als sekundäre Hyperalgesie bezeichnet. [12,13]
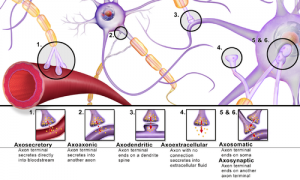
verschiedene Synapsen aus wikipedia.org
Sie dient der gezielteren Informationsübertragung zweiter benachbarten Zellen, wobei konvergierende (mehrere Zellen treffen auf weniger Rezeptoren) und divergierende (umgekehrt) Effekte auftreten. Der präsynaptische Effektor einer Zelle ist meist am Ende aufgetrieben (Endkolben) und enthält zahlreiche Vesikel und Mitochondrien für die Bereitstellung des bzw. der Signalstoffe. Der postsynaptische Rezeptor (s.o.) befindet sich in einer spezielleren Membran und hat in einer Nervenzelle zahlreiche Verbindungen über Transport-Systeme wie Filamente. Er befindet sich entweder in einem Dendrit, einem Axon bzw. Neurit oder Soma eines Neurons. Er wirkt dann hemmend oder erregend. Weitere Synapsen bzw. postsynaptische Rezeptoren findet man in Drüsen-, Muskel- und Immunzellen. [3]
In ZNS findet man cholinerge, noradrenerge, dopaminerge, serotonerge, GABA-erge, glutaminerge, histaminerge und peptiderge (Neuropeptid Y) Synapsen. Im VNS überwiegen im sympathischen Teil cholinerge (v.a. nikotinerge) präganglionär und an Schweißdrüsen sowie α2-adrenerge Synapsen postganglionär. Im parasympathischen System dominieren cholinerge Synapsen vom nicotinergen und muscarinergen Typ. (Anatomie des vegetativen Nervensystems)
Die motorische Endplatte stellt als Sonderform die informative Verbindung von Nerv zu quergestreifter bzw. Skelett-Muskulatur und anderen Muskelzellen dar. An glatter Muskulatur findet man Natrium-Kalzium-Kanäle, adrenerge (α1, β-Rezeptoren), cholinerge (muscarinerge Rezeptoren vom Typ M1-5) und peptiderge bzw. Y1-Rezeptoren (Transmitter hier Neuropeptid Y). Am Magen-Darm-Trakt sind es v.a. muskarinerge Rezeptoren von Typ M3.
Forschungen haben ergeben, dass Lokalanästhetika nicht nur den ionotropen Rezeptor am Transport von Natrium und Kanal reversibel hindern (örtliche Betäubung), sondern auch „alternative“ Effekte an Zellen hervorrufen, welche nur über metabotrope Rezeptoren verfügen. Sie wirken u.a. über muscarinerge und G-Protein-gekoppelte Rezeptoren an glatten Muskelzellen, Leukozyten, Thrombozyten u.v.a.m. [14,15]